
Directorio de Establecimientos Sin Gluten
Encuentra establecimientos y restaurantes con opciones deliciosas, ¡sin gluten!

Directorio de alimentos
Accede al directorio de productos y alimentos

Directorio de Establecimientos Sin Gluten
Encuentra establecimientos y restaurantes con opciones deliciosas, ¡sin gluten!

Directorio de alimentos
Accede al directorio de productos y alimentos
Publicado el: 6 de febrero de 2026
La Universidad de Tampere acogió el pasado mes de septiembre la cuarta edición de su Simposio de Enfermedad Celíaca, que tiene lugar cada dos años y reúne en esta ciudad de Finlandia a los médicos e investigadores más relevantes a nivel mundial. Está organizado por la Sociedad Internacional para el Estudio de la Enfermedad Celíaca (ISSCD), que fue fundada y registrada en los Países Bajos en 2011 y que actualmente cuenta con 900 socios.
La Sociedad Internacional para el Estudio de la Enfermedad Celíaca (ISSCD, International Society for the Study of Celiac Disease) cuenta con diferentes comités para abordar los retos actuales relacionados con la enfermedad celíaca (EC) y la dieta sin gluten. En base a ellos se estructuró el programa de contenidos, que resumimos aquí con lo más relevante.
Factores implicados en el desarrollo de la enfermedad celíaca
Los grandes estudios prospectivos observacionales y de intervención que se han llevado a cabo con miles de bebés con predisposición a EC han arrojado mucha luz sobre los fenómenos que acontecen antes de manifestarse la enfermedad y los posibles factores implicados en su debut. Un ejemplo es el estudio de intervención PreventCD que, como expuso Carolina Meijer-Boekel (Universidad de Leiden, Países Bajos), demostró que la lactancia materna y la edad de introducción de cereales con gluten en los bebés con predisposición genética no influyen en el riesgo posterior de desarrollo de la EC, a diferencia de lo que se pensaba.
Otro ejemplo lo mostró Maureen Leonard (Universidad de Harvard, Boston, Estados Unidos). Se trata del estudio observacional CDGEMM (Celiac Disease Genomic Environmental Microbiome and Metabolome study), que ha recopilado datos genéticos, microbiológicos y diversos marcadores en bebés con predisposición a EC desde el nacimiento y ha podido comprobar una interesante secuencia temporal de acontecimientos antes del debut de la EC. Más de 18 meses antes de manifestarse la EC ya se produce una disbiosis intestinal, hacia el mes 18 previo al diagnóstico se observa un aumento de zonulina (marcador de aumento de permeabilidad intestinal), 9 meses antes se produce elevación de anticuerpos antipéptidos desamidados de gliadina en sangre y en los últimos 6 meses antes del diagnóstico tiene lugar algún fenómeno que altera la ya desequilibrada microbiota intestinal y es entonces cuando por fin se elevan en sangre los anticuerpos antitransglutaminasa revelando que la EC ya está en marcha.
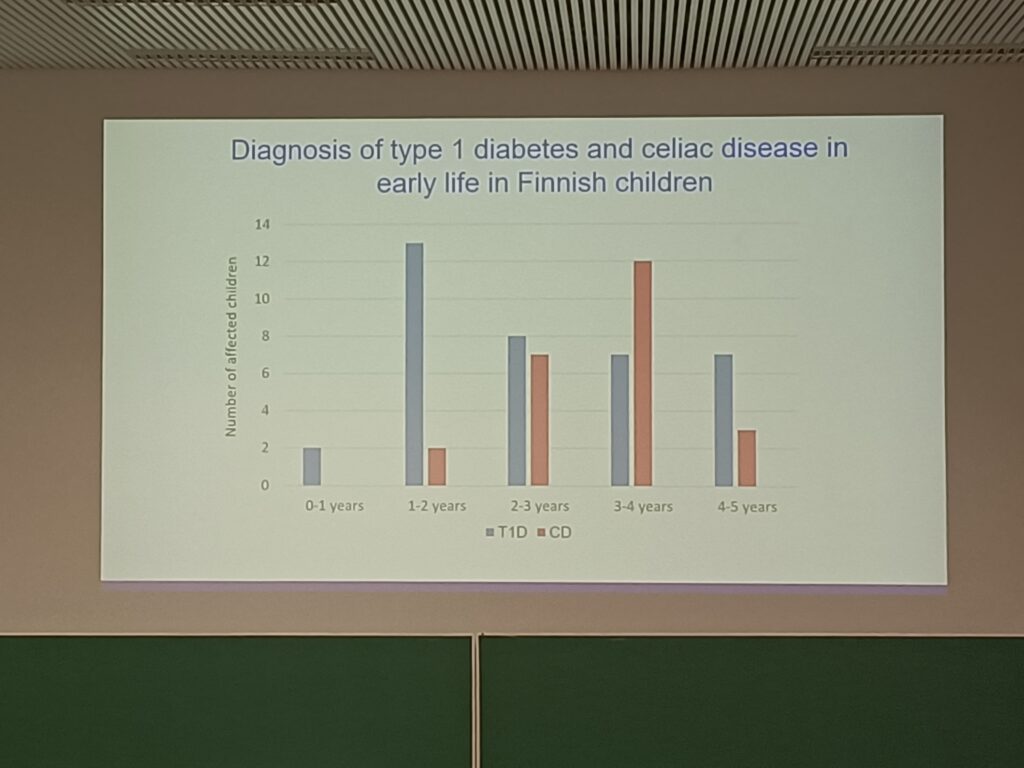
Por su parte, Mikael Knip (Universidad de Helsinki, Finlandia) explicó cómo los estudios combinados de EC y diabetes tipo 1 han mostrado que los bebés con la combinación de riesgo HLA DR4-DQ8 presentan marcadores de autoinmunidad a edades muy tempranas (1-2 años), concretamente autoanticuerpos anti-insulina, mientras que los que presentan la combinación HLA DR3-DQ2 tardan más en mostrar rasgos de autoinmunidad, en este caso anticuerpos anti-GAD. Estos datos muestran que el proceso autoinmune que conducirá finalmente a una diabetes tipo 1 se inicia muy pronto, mientras que la manifestación clínica de la enfermedad llega más tarde, a los 8 años de edad como media. Y aquellos pacientes en los que coexiste la diabetes tipo 1 con la EC, ésta se manifiesta en promedio 6 meses después de que se haya manifestado la diabetes.
Así lo expresó también Heiki Hyöty (Universidad de Tampere, Finlandia), quien destacó que en la diabetes tipo 1 no hay un claro detonante, como lo es el gluten en la EC, aunque las infecciones por los mismos tipos de virus pueden contribuir al desarrollo de ambas, especialmente los enterovirus. En el 60%-80% de los casos de diabetes tipo 1 se detecta la presencia de fragmentos proteicos y genéticos de enterovirus en las células del páncreas, especialmente del virus Coxsackie B. En EC, además de los enterovirus se han postulado como posibles detonantes las infecciones digestivas por rotavirus, reovirus y parechovirus, e incluso infecciones respiratorias por adenovirus y rinovirus.
El estudio TEDDY, que comenzó hace más de 2 décadas a reclutar bebés con predisposición genética a EC y diabetes tipo 1 y que ha seguido a los miles de participantes hasta la edad de 15 años, ha creado una rama paralela de investigación, el estudio MAVRIC, para analizar en las muestras de sangre recolectadas la presencia de anticuerpos contra estos tipos de virus antes del desarrollo de la EC y/o de la diabetes tipo 1. Se trata de averiguar mecanismos que detonan estas enfermedades, como puede ser la persistencia de la infección a nivel de la mucosa intestinal, y de evaluar la posibilidad de desarrollar estrategias preventivas contra la EC y la diabetes, ya sea la inmunización frente a estos virus para evitar la infección o la erradicación farmacológica de la infección cuando ésta se cronifica.
En el apartado genético, Iris Jonkers (Universidad de Groningen, Países Bajos) recordó que los genes HLA explican en torno al 40% de la base genética de la EC y los 57 marcadores genéticos identificados hasta la fecha fuera del sistema HLA aportan alrededor de un 15% de riesgo adicional. Más del 95% de estas variantes adicionales de riesgo se encuentran fuera de los genes, en regiones no codificantes, que afectan a la expresión de diferentes genes y cuyo impacto puede ser diferente de unos tipos celulares a otros. Son datos obtenidos de más de 2,2 millones de muestras genotipadas en diferentes estudios y compartidas en biobancos. El marcador genético que más se repite entre los diferentes estudios y se considera el más asociado se encuentra en la región genética que alberga los genes de las sustancias inflamatorias IL2/IL-21.
Y en cuanto a la microbiota intestinal, las investigaciones del grupo de Elena Verdú (Universidad de McMaster, Hamilton, Canadá) han demostrado que las bacterias de los géneros Lactobacillus y Pseudomonas pueden metabolizar el gluten, pero lo hacen de manera diferente y el resultado de ello también es diferente si están aisladas o en comunidad. Pseudomonas genera fragmentos de gluten más tóxicos. Si Lactobacillus está presente, los metaboliza reduciendo su toxicidad. Por otro lado, la manera de metabolizar el triptófano de la dieta, actividad en la que participan tanto enzimas digestivas humanas (por dos vías, la de la kinurenina y la de la serotonina) como enzimas microbianas del ambiente intestinal, influye en el estado inflamatorio del intestino según los grupos bacterianos presentes. La vía microbiana, con la generación de indoles, contribuye a la desinflamación intestinal. Y también contribuye a reducir la inflamación la metabolización de fibras vegetales complejas con la generación de ácidos grasos de cadena corta. En ello son especialistas las bacterias del grupo Prevotella, que se encuentra reducido en la microbiota intestinal de las personas con EC. Las alteraciones de la microbiota intestinal ya están presentes antes de que la EC se manifieste, según se extrae del estudio prospectivo de las heces de bebés con predisposición genética, analizadas cada 4 meses desde los 0 hasta los 4 años.
Con todo, los factores no modificables que más influyen en el riesgo de desarrollar la EC son, en palabras de Daniel Agardh (Universidad de Lund, Suecia), la genética HLA, el sexo femenino y una historia familiar de EC. Así, una niña con doble carga genética de la variante de riesgo HLA-DQ2 y con un familiar de primer grado con EC tiene un 25% de posibilidades de desarrollar la EC. También influye la estación del año en la que se produce el nacimiento, con un mayor riesgo de desarrollo de EC en los nacidos en primavera y verano. Y los factores modificables, de tipo ambiental, son la ingesta de gluten y las infecciones digestivas. El riesgo de desarrollo de la EC se incrementa si la ingesta de gluten es elevada en los primeros 5 años de vida y se producen infecciones digestivas por enterovirus en los primeros 2 años de vida.
Variabilidad clínica de la enfermedad celíaca
En la infancia, según resumió Peter Green (Universidad de Columbia, Nueva York, Estados Unidos), son 3 las situaciones clínicas fundamentales que conducen al diagnóstico de la EC: el dolor abdominal (22% de los casos), los problemas de crecimiento (26%) y el cribado de la enfermedad (52%) por diferentes motivos que hacen sospechar la enfermedad, ya sean manifestaciones extradigestivas (sobre todo dermatológicas y neurológicas), alteraciones analíticas, enfermedades autoinmunes asociadas o familiares de primer grado afectados por la enfermedad.
En adultos, la manifestación inicial que da pie al diagnóstico es la diarrea (36% de los casos), la anemia (13%) o los problemas óseos (5%). En un 20% de los casos la sospecha de la enfermedad nace de otras alteraciones analíticas y problemas extradigestivos asociados, un 8% son detectados por cribado familiar y el 4% se detecta de manera casual, a veces tras una endoscopia realizada por otro motivo.
El origen de la diarrea no tiene que ver con el grado de afectación del intestino ni con el tramo intestinal dañado. Puede ser debida a una insuficiencia pancreática, a una intolerancia a ciertos nutrientes (azúcares, FODMAP) o a problemas digestivos añadidos como el sobrecrecimiento bacteriano (SIBO), alteraciones de la motilidad intestinal o la colitis microscópica.
Existe además un sesgo por sexos, de forma que en varones es más frecuente que se encuentre infradiagnosticada y que presente síntomas y alteraciones analíticas como la anemia de manera más severa (en comparación con las mujeres), o que presenten una menor estatura (en comparación con varones sanos). A pesar de todo, el cuadro de síntomas que presenta una persona antes del diagnóstico no es predictivo de EC, ya que se puede presentar igualmente en personas sin EC.

Dermatitis herpetiforme
La dermatitis herpetiforme es una manifestación cutánea exclusiva de la EC que tiene entidad propia como enfermedad, a ella dedicó Teea Salmi (Universidad de Tampere, Finlandia) su intervención. Provoca erupciones de picor intenso en la piel que se localizan en los codos (85% de los casos), el sacro (54%) y las rodillas (49%), llegando a extenderse en ocasiones hasta los hombros (27%) y la cara (15%).
Se diagnostica preferentemente en la quinta década de la vida, probablemente porque se trata de casos de EC no detectados anteriormente. Sólo un tercio de los casos presentan síntomas digestivos, aunque en las pruebas analíticas se detecta anemia en el 12% de estos pacientes y elevación de anticuerpos antitransglutaminasa en el 95%. La biopsia duodenal revela atrofia vellositaria en el 75% de los casos y aumento de linfocitos intraepiteliales del subtipo gamma-delta en el 91%. La dermatitis herpetiforme se confirma evaluando la presencia de depósitos de IgA en biopsias de piel sana.
El tratamiento es la dieta sin gluten, acompañada en los primeros meses de un fármaco, la Dapsona, que elimina rápidamente el picor y la lesión cutánea. A pesar de ello, un 11% de los pacientes presentan algún síntoma cutáneo una vez al mes y llega a haber persistencia de molestias digestivas en el 14% de los que presentaban síntomas intestinales. El 4% de las mujeres y el 13% de los varones afectados mantienen el tratamiento con Dapsona a largo plazo, pese a las contraindicaciones.
La dermatitis herpetiforme se asocia con la diabetes tipo 1, la tiroiditis autoinmune y con un mayor riesgo de fracturas, pero en menor medida que en el resto de los pacientes con EC. El pemphigus vulgaris, en cambio, sí es más frecuente en los casos de EC con dermatitis herpetiforme. No se han vinculado daños renales ni posibles infecciones como desencadenantes de la dermatitis herpetiforme.
Manifestaciones neurológicas relacionadas con el gluten
Las manifestaciones neurológicas relacionadas con el gluten representan un caso particular y de los más reseñables entre las manifestaciones extradigestivas que se pueden dar en la EC porque trascienden la propia EC y se presentan de igual manera en pacientes con y sin EC. El mayor experto en este campo es Marios Hadjivassiliou (Hospital de Sheffield, Reino Unido) con el estudio de una cohorte nada desdeñable que supera los 2.000 pacientes con trastornos neurológicos causados por el gluten. El 60% corresponden a ataxia, el 23% son neuropatías periféricas (pérdida de sensibilidad en extremidades, en ocasiones dolor) y el 17% se deben a encefalopatías (migrañas, confusión mental, etc.). No todos los casos se someten a una biopsia intestinal para confirmar la EC y se estima que sólo el 28% de estos pacientes tienen EC.
Seguimiento de la enfermedad celíaca
Seguimiento en la edad pediátrica
En edad pediátrica, tal como expuso Valentina Discepolo (Universidad de Nápoles, Italia), se recomiendan 2-3 controles médicos el primer año (meses 3, 6 y 12) y después controles cada 1-2 años, siempre con el pediatra gastroenterólogo o con el nutricionista experto en EC. Se debe evaluar la evolución de los signos y síntomas de la EC así como el crecimiento, y en sangre cualquier parámetro que estuviese alterado en el momento del diagnóstico, además de los anticuerpos. Hay que tener en cuenta que la adherencia a la dieta sin gluten decae con la edad. Si todo va bien, la situación debe estar normaliza en el plazo de 6-12 meses. Si no es así, especialmente si existe retraso de crecimiento o retraso puberal, es aconsejable la evaluación por parte de un endocrino. La restricción de lactosa debe ensayarse sólo si existen síntomas compatibles (gas, dolor y distensión abdominal, diarrea). El síndrome de intestino irritable se da con igual frecuencia en niños con o sin EC.
En los casos que requieran confirmación diagnóstica tras haber instaurado la dieta sin gluten, será necesaria una reintroducción de gluten en la alimentación, la conocida como prueba de provocación. La pauta es administrar 10-15 gramos de gluten al día durante 3-6 meses. La aparición de síntomas y la elevación de anticuerpos en sangre son suficientes para confirmar el diagnóstico, sin excluir la biopsia intestinal si existen dudas. Tiempos más cortos de provocación o cantidades alternativas no están aún bien definidas y no se recomiendan.
En cuanto a la EC potencial (elevación de anticuerpos en sangre con biopsia normal), se aconseja mantener el gluten en la dieta si no hay síntomas y hacer un seguimiento anual, repitiendo la biopsia en el momento en el que se presenten síntomas. Es decisión de los padres realizar la biopsia si no se presentan síntomas durante este seguimiento pero los anticuerpos persisten en valores positivos. En los casos de EC potencial con síntomas se suele optar por retirar el gluten de la dieta. Se estima que la EC potencial representa el 20% del total de casos de EC en pediatría.
Seguimiento en la edad adulta
Katri Kaukinen (Universidad de Tampere, Finlandia) comentó que un tercio de los pacientes adultos aún no están recuperados transcurrido 1 año desde el diagnostico, y el 2-4% siguen estando mal hasta 10 años después del diagnóstico. Estos casos son considerados ‘lentos respondedores’ y se dan con más frecuencia en varones mayores de 45 años que presentaron síntomas más severos en el momento del diagnóstico o que tienen patologías asociadas (intolerancias alimentarias adicionales u otros problemas digestivos, así como patologías autoinmunes como la tiroiditis autoinmune). En general, responden mejor a la dieta sin gluten quienes manifestaron la EC con síntomas extradigestivos. Un resultado negativo en la analítica de anticuerpos no es garantía de recuperación, la mitad de los casos con atrofia persistente muestran valores negativos de anticuerpos en sangre.
La periodicidad establecida para los controles de la enfermedad varía de unas guías a otras, pero en general son bastante concordantes. La Asociación Americana de Gastroenterología (AGA) y la Sociedad Británica de Gastroenterología (BSG) recomiendan controles médicos anuales, y controles dietéticos sólo si se sospechan errores en la dieta sin gluten. La Sociedad Europea para el Estudio de la EC (ESsCD) establece 3 controles médicos el primer año (meses 3-4, 6 y 12), dos controles anuales después (años 2 y 3) y luego ya controles cada 1-2 años; a nivel dietético plantea dos controles el primer año (meses 4-6 y 12). Por su parte, la Organización Mundial de Gastroenterología (WGO) marca controles médicos cada 1-2 años desde el diagnóstico y controles dietéticos cada 1-2 años, con dos revisiones en el primer año (meses 4-6 y 12). En todos los controles se deben valorar en sangre los anticuerpos específicos de la EC y la biopsia de seguimiento sólo está sugerida por la WGO el primer año, las demás guías la condicionan al estado de salud de cada paciente.

Complicaciones de la enfermedad celíaca
Alberto Rubio-Tapia (Clínica Cleveland, Estados Unidos) habló de las complicaciones hepáticas y óseas en la EC. La EC está presente en el 9% de casos con elevación de enzimas hepáticas en sangre, en el 4-6% de casos con hepatitis autoinmune, en el 3-7% de pacientes con NASH y en el 5% de personas con cirrosis criptogénica. No es necesario realizar biopsia de hígado en pacientes celíacos con alteraciones hepáticas si éstas se resuelven en el plazo aproximado de 1 año. Si persisten, la biopsia hepática es oportuna para confirmar una posible hepatitis crónica autoinmune, especialmente si existe elevación de enzimas hepáticas y de anticuerpos antinucleares (ANA).
Por otra parte, el 30-60% de pacientes con EC tienen osteopenia y el 14-35% osteoporosis. Ello multiplica por 1,4-2,5 el riesgo de fractura de huesos. Los datos indican que es relevante analizar la densidad mineral ósea en personas celíacas mayores de 45 años con bajo peso o con pérdida de peso. En el resto, la desmineralización del hueso es equiparable a la de la población general. No obstante, no existe consenso y diferentes guías ofrecen diferentes recomendaciones. La Asociación Americana de Gastroenterología (AGA) recomienda analizar la densidad mineral ósea en todas las personas celíacas adultas en el momento del diagnóstico, mientras que la Sociedad Europea para el Estudio de la EC (ESsCD) lo recomienda si la persona tiene 35 años o más al ser diagnosticada. Por su parte, las guías clínicas del Reino Unido (NICE) recomiendan este análisis en adultos con factores de riesgo y la Sociedad Británica de Gastroenterología (BSG) lo acota a mayores de 55 años con factores de riesgo.
La complicación más grave, la EC refractaria, fue expuesta por Luca Elli (Policlínico de Milán, Italia). Se define por la persistencia de atrofia vellositaria acompañada de síntomas y signos de malabsorción a pesar de la dieta sin gluten. Existen dos tipos de EC refractaria que se diferencian por el porcentaje de linfocitos T aberrantes (por debajo del 20% el tipo 1 y por encima el tipo 2) y por la variabilidad de su receptor TCR (policlonal en el tipo 1, monoclonal en el tipo 2). La EC refractaria tipo 2 se considera una fase inicial de un linfoma intestinal de células T que tiene mal pronóstico y que suele manifestarse en el yeyuno y el íleon más que en el duodeno, por lo que se opta por la cápsula endoscópica para detectarlo en lugar de biopsias aleatorias que raramente alcanzan esos tramos intestinales. La elevación de anticuerpos antitransglutaminasa en sangre no excluye que pueda tratarse de una EC refractaria, pero hay que considerar también una posible mala adherencia a la dieta sin gluten. La ausencia de anticuerpos en estos casos sí debe hacer sospechar una EC refractaria.

Evolución de la enfermedad celíaca con la dieta sin gluten
La dieta sin gluten es el único tratamiento para la EC y, como indicó Daniel Leffler (Centro Médico Beth Israel Deaconess, Boston, Estados Unidos), es eficaz si se realiza de manera estricta y continuada, pero es fundamental monitorizar su evolución. Se considera que existe buena respuesta a la dieta sin gluten cuando se confirma la resolución de los síntomas y la negativización de los valores analíticos de anticuerpos, junto con la reparación de la lesión intestinal, alcanzándose un estado nutricional adecuado y un buen nivel de calidad de vida. La normalización de síntomas y de anticuerpos no es garantía de plena recuperación, ya que entre un 30% y un 60% de personas celíacas siguen mostrando daño intestinal dos años después del diagnóstico a pesar de no tener síntomas ni anticuerpos.
Cuando persisten los síntomas, los anticuerpos o la lesión intestinal se habla de EC no respondedora. En palabras de Govind Makharia (Instituto de Ciencias Médicas All India, Nueva Delhi, India), se estima que ocurre en el 22% de los pacientes. La primera causa de esta situación a considerar es el mal cumplimiento de la dieta sin gluten. Para ello, continuó Anne Roland Lee (Universidad de Columbia, Nueva York, Estados Unidos), son útiles las herramientas que evalúan el grado de adherencia a la dieta sin gluten, como los registros, los cuestionarios o las entrevistas dietéticas, y pruebas cuyos resultados pueden revelar la ingesta de gluten, como el análisis de anticuerpos en sangre o el análisis de gluten en heces u orina. La ingesta de gluten explica un tercio de los casos de mala evolución, sin olvidar que hay pacientes ultrasensibles que reaccionan ante mínimas cantidades de gluten que están dentro de los límites legales y que son toleradas por la mayoría de los pacientes.
Descartada la ingesta de gluten, Fabiana Zingone (Universidad de Padua, Italia) comentó que es necesario revisar el diagnóstico inicial, es erróneo en un 7% de los casos, e investigar otros problemas digestivos como el síndrome de intestino irritable, responsable de la falta de respuesta en el 16% de los casos. Otras posibles causas son el sobrecrecimiento bacteriano (6%), la colitis microscópica (6%) o la intolerancia a azúcares como lactosa y fructosa (5%).
En el caso de persistencia de atrofia, observada hasta en el 48% de casos tras 5 años de dieta sin gluten y en el 56% de pacientes mayores de 70 años, según datos de Georgia Malamut (Universidad de la Ciudad de París, Francia), es necesario descartar también causas farmacológicas (toxicidad por micofenolato, olmesartán) y patologías como la inmunodeficiencia común variable y la enteropatía autoinmune. Excluidas éstas y otras causas de no mejoría, en el peor (y menos frecuente) de los casos puede tratarse de una EC refractaria que requerirá tratamiento inmunosupresor.
Nadine Cerf-Bensussan (Universidad de la Ciudad de París, Francia) habló también de la EC refractaria (ECR), que se caracteriza por síntomas de malabsorción con persistencia de atrofia vellositaria y aumento de linfocitos intraepiteliales, con un fenotipo normal (CD103+ CD8+ TCRab+ en superficie) en la ECR tipo 1 y un fenotipo aberrante (si supera el 20%), con los marcadores CD8 y TCR intracelulares, en la ECR tipo 2, considerada una fase premaligna de linfoma intestinal de células T. La tinción inmunohistoquímica no diferencia entre ambos fenotipos, la citometría de flujo sí.

¿Cuál es realmente la dosis de gluten tolerada?
La Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO, Food and Agriculture Organization) lidera los esfuerzos para combatir el hambre en el mundo, tal como relató Kang Zhou, experto en Seguridad Alimentaria de la FAO. El objetivo último es proporcionar el acceso a alimentos seguros y suficientes en cantidad y calidad. Las normas de calidad y guías de buenas prácticas para la producción y comercio internacional de alimentos son elaboradas desde 1963 por la Comisión del Codex Alimentarius, surgida del programa conjunto de la FAO y la Organización Mundial de la Salud (OMS) para garantizar la salud de los consumidores.
La primera norma recogida en el Codex relativa a la seguridad de los consumidores con EC se remonta a 1979 (CXS 118-1979) y en ella se define por primera vez qué es el gluten, en qué cereales se encuentra, qué alimentos son seguros y cuáles no, cuál es el límite máximo de gluten admitido en los alimentos destinados a consumidores con enfermedad celíaca (intolerancia al gluten en su definición original) o cómo declarar su presencia. El texto original fue modificado con una enmienda en 1983 y otra en 2015, tras una revisión en 2008.
La Comisión del Codex cuenta con 10 comités para regular los aspectos más generales y dos de ellos afectan de forma específica a la EC, uno relacionado con la higiene alimentaria (CCFH, Codex Committee on Food Hygene) y otro con el etiquetado de alimentos (CCFL, Codex Committee con Food Labeling). Entre 2020 y 2024 se han celebrado 5 reuniones para redefinir el concepto de alérgeno y diferenciar así la EC de las alergias alimentarias, quedando definido el alérgeno como una sustancia capaz de desencadenar reacciones inmunomediadas, ya sean alergias alimentarias mediadas por IgE o enfermedad celíaca.
En el caso que nos ocupa, el alérgeno no sería el gluten como tal sino de forma genérica los ‘cereales que contienen gluten’ y queda por definir la dosis de alérgeno segura. Para las personas celíacas está establecida en 20 miligramos de gluten por kilo de alimento (20 partes por millón, ppm), límite adoptado en la mayoría de los países que han legislado al respecto, pero es necesario ajustar la dosis tolerada por las personas alérgicas de forma que se eviten etiquetados ambiguos o contradictorios, en los que figure la mención ‘sin gluten’ y a la vez la advertencia ‘puede contener trazas de gluten’.
Existe un comité científico de expertos en los campos de la microbiología, los pesticidas, los aditivos alimentarios, la nutrición y los alérgenos alimentarios que asesoran a la Comisión del Codex y son los encargados en este caso de traducir los datos clínicos sobre el nivel de tolerancia de personas celíacas y alérgicas al gluten a una dosis de referencia que marque el límite de seguridad.
La dosis máxima de cada alérgeno se establece en base al coeficiente EDp (Eliciting Dose predicted), que equivale a la dosis de alérgeno que provocaría una reacción adversa en el 1% (EDp01) o en el 5% (EDp05) de la población alérgica. En el caso del gluten existe consenso en utilizar el límite EDp05 (es decir, el 95% de los alérgicos no sufrirían reacción alguna) al no haberse documentado reacciones serias y teniendo en cuenta las limitaciones técnicas y metodológicas de la industria alimentaria a la hora de prevenir la contaminación y de los métodos analíticos a la hora de detectar trazas de alérgenos.
Para Jennifer Sealey-Voyksner (Compañía ImmunogenX, Los Ángeles, Estados Unidos) el reto es conocer el mecanismo por el que pequeñas dosis de gluten resultan dañinas para algunos pacientes, los definidos como ultrasensibles al gluten (una única dosis de 3 miligramos de gluten puede activar la respuesta inflamatoria, medida por la elevación del marcador IL-2 en sangre a las 4 horas de la ingesta), y marcar un límite de gluten que sea seguro para la amplia mayoría de los pacientes. Está pendiente igualmente definir bien los parámetros más indicados para evidenciar la exposición al gluten y establecer protocolos válidos y clínicamente asumibles en las pruebas de provocación.
Según las investigaciones de Robert Anderson (Universidad de Melbourne, Australia) con pacientes, la reacción se desencadena de la misma manera tanto si el gluten es administrado por vía oral (10 gramos de gluten vital, con un 75% de proteína y un bajo contenido en fructanos) o mediante inyección intradérmica (miligramos), generando en ambos casos síntomas similares y la liberación de las mismas citoquinas. Los síntomas, además, se atenúan al administrar dosis repetidas. Para él, la EC es desde el punto de vista inmunológico una hipersensibilidad de tipo IV, protagonizada por una respuesta de células T específicas de gluten.
Desde el punto de vista de la industria dedicada al desarrollo de métodos analíticos, la cuestión que planteó Markus Lakorn (Compañía R-Biopharm, Darmstadt, Alemania) es si queda algo por hacer, ya que en el mercado ya hay métodos analíticos de gluten sólidamente validados que cumplen con la necesidad de garantizar la salud de los pacientes. Sin embargo, queda por definir bien qué es el gluten en términos analíticos. La normativa actual establece de forma general que un resultado analítico de gluten debe multiplicarse por dos para establecer el contenido en esta proteína, asumiendo que las gliadinas (componente del gluten detectado por los métodos analíticos) se encuentran en igual proporción que las gluteninas (componente del gluten no detectado por los métodos analíticos). La realidad es que la proporción gliadinas:gluteninas no es de 1:1 sino de 2:1 en el caso del trigo, por lo que el resultado debería multiplicarse por 1,5 y no por 2. En el caso del centeno el factor multiplicador oscilaría entre 1,12 y 1,16, y en la cebada entre 1,20 y 1,71 para que el resultado fuera más fiel a la realidad. Esto sugiere que actualmente se está sobreestimando el contenido en gluten de los alimentos, que en realidad contendrían menos de lo que se indica tras una analítica.
Y desde la perspectiva de la industria alimentaria, representada en esta ocasión por Fabiana Saorin y Daniele Grano (Compañía Dr. Schär, Postal, Italia), se admite que ya es posible elaborar productos sin gluten garantizando niveles de gluten muy por debajo de los actuales 20 mg/kg, pudiendo llegar a cumplir con los límites de 10 ppm o hasta 5 ppm e incluso 3 ppm, que son los que marcan los países con legislaciones más restrictivas, como Argentina, Chile, Australia o Nueva Zelanda.

Terapias farmacológicas en estudio
Cada vez hay más compañías farmacéuticas involucradas en el desarrollo de tratamientos farmacológicos que complementen la dieta sin gluten en los casos que no terminan de mejorar, que oscilan entre el 12% y el 34% según diferentes estudios que comentó Jorma Isola (Universidad de Tampere, Finlandia).
No es una tarea sencilla y uno de los requerimientos de la FDA (Food and Drug Administration), organismo regulador del desarrollo farmacológico en Estados Unidos, es que se disponga de escalas de medida objetivas que permitan valorar la mejoría de la enfermedad con el tratamiento experimental. La clasificación de la lesión intestinal según la escala de Marsh-Oberhüber es bastante fiable con lesiones serias (Marsh 2-3) pero no lo es tanto con lesiones leves (Marsh 0-1), que son las que más se suelen ver en los participantes en ensayos clínicos, que son personas que no terminan de mejorar y de ahí que sean reclutadas en los ensayos que persiguen resolver estos casos con fármacos.
Michael Schumann (Universidad de Mainz, Alemania) hizo un repaso de algunos de ellos. El inhibidor de transglutaminasa ZED1227 continúa con sus ensayos en fase 2, y entre las nanopartículas encaminadas a inducir tolerancia inmunológica frente al gluten, TPM502 ha ofrecido resultados prometedores en los ensayos de fase 1 mientras que TAK101 no ha mostrado efectos diferentes a los observados con el placebo. Por su parte, los ensayos con la terapia oral con proteasas TAK062 han sido interrumpidos en la fase 2. Las terapias inmunológicas son objeto también de intensa investigación y fármacos experimentales como IMU856 o Caly002 siguen adelante de forma satisfactoria.
Una de las terapias inmunológicas que se suma a las ya en marcha es FB102, basada en un anticuerpo monoclonal dirigido específicamente contra CD122, que es la subunidad que comparten los receptores de las interleuquinas IL-2 e IL-15, principales agentes inflamatorios en la EC. El objetivo es que el fármaco, presentado por Jason Tye-Din (Universidad de Melbourne, Australia), bloquee la acción inflamatoria de estas citoquinas al ingerir gluten. Los ensayos en fase 2 se iniciaron en agosto de 2025.

Nuevos biomarcadores de enfermedad celíaca
Jason Tye-Din (Universidad de Melbourne, Australia) presentó también uno de los nuevos marcadores que centran el interés clínico y científico en la EC, la interleuquina 2 (IL-2). Se trata, junto con el interferón gamma (IFNg), de una de las moléculas promotoras de inflamación que se liberan en la EC tras la ingesta de gluten y es producida por las células T específicas de gluten. Se ha comprobado que una ingesta puntual de 3 gramos de gluten en una persona celíaca que ya se encuentra a dieta sin gluten provoca una elevación de IL-2 en sangre detectable a las 2-4 horas de la ingesta, fruto de la activación de las células T de memoria específicas de gluten.
Al margen de las implicaciones clínicas que ello tiene, ya que puede ayudar a confirmar la EC en pacientes que iniciaron la dieta sin gluten sin tener claro el diagnóstico, es indudable la aplicación de este hallazgo en la investigación farmacológica. Anteriormente se comentó lo estricta que es la FDA para autorizar los ensayos clínicos. Otro de sus requisitos es que se pueda evaluar la respuesta sintomática de los pacientes a los tratamientos experimentales. No siempre es fácil determinar si los síntomas que presenta una persona con EC son atribuibles al gluten o a otros factores. La determinación de IL-2 en sangre ayudaría a adjudicar al gluten la aparición de ciertos síntomas.
Por otro lado, el estudio de este marcador ha revelado igualmente que algunos pacientes reaccionan frente a granos sin gluten como el mijo o el césped inglés, al menos en cuanto a la activación inmunológica en la que interviene la IL-2. En los ensayos realizados, 4 pacientes reaccionaron de esta manera al consumo de 100 gramos de pan elaborado con harina de mijo, lo que equivale a la ingesta de 4,9 gramos de proteína no-gluten.
Autor: Juan Ignacio Serrano Vela. Doctor en Biología. Servicio de Investigación de la Asociación.

